Skupenské změny
[Edit]- Úvod
- Tání
- Tuhnutí
- Změna objemu těles při tání a tuhnutí
- Sublimace a desublimace
- Vypařování a kondenzace
- Fázový diagram
- Vodní pára v atmosféře
Úvod
táž látka se může vyskytovat jako plynný kapalná nebo pevná
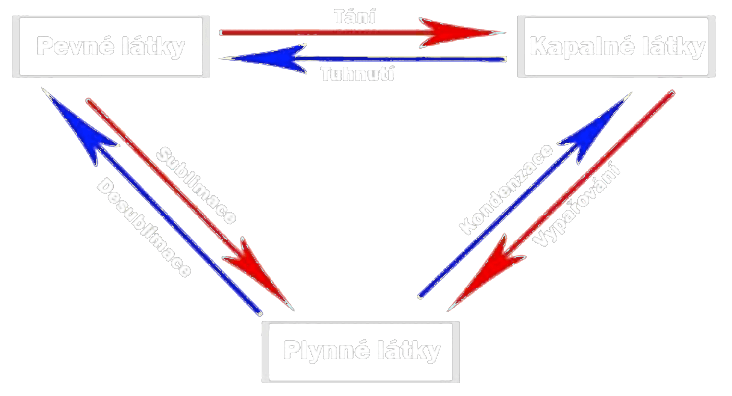
Tání
K tání dochází při zahřívání krystalické látky. Pokud teplota látky dosáhne teploty tání, pevná krystalická látka se mění na kapalinu. Různé krystalické látky mají také různou teplotu tání, pro danou látku závisí teplota tání na vnějším tlaku, při kterém tání probíhá.
Teplota tání krystalické látky závisí na tlaku okolního prostředí. U látek, u nichž je tání doprovázeno zvětšením objemu, roste při zvýšení tlaku také teplota tání. Je-li tání doprovázeno zmenšením objemu, pak se při zvýšení vnějšího tlaku sníží teplota tání látky.
Amorfní látky – u těchto látek nedochází ke klasickému tání, tyto látky postupně měknou, až se přemění na kapalinu. Př. vosk, sklo, asfalt.
Některé látky se nemohou zahřát až k teplotě tání, protože již při nižší teplotě se rozkládají. Př. dřevo, mramor
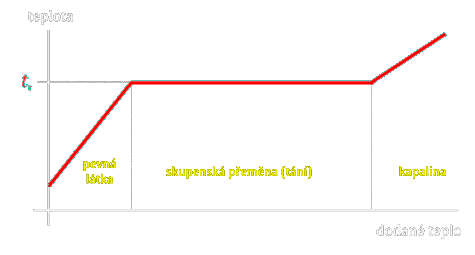
Skupenské teplo tání
Teplo, které přijme pevná látka již zahřátá na teplotu tání, aby se změnila na kapalinu téže teploty. Jednotkou je [J]
Měrné skupenské teplo tání
Teplo, které musíme dodat 1 kg látky, aby změnila své skupenství z pevného na kapalné. Jednotkou je [J.kg]
Tuhnutí
Fyzikální děj, při kterém se mění skupenství látky z kapalného na pevné. Skupenské teplo tuhnutí je stejné jako skupenské teplo tání, pouze se jedná o teplo, které látka odevzdá svému okolí. Při tuhnutí nevzniká pevné skupenství okamžitě. Když dosáhne kapalina teploty tuhnutí, tak se v kapalině začnou vlivem vazebných sil vytvářet krystalizační jádra = zárodky. Pokud se vytvoří pouze jeden zárodek a částice látky se k němu postupně připojují, tak vznikne monokrystal.
Změna objemu těles při tání a tuhnutí
Většina látek při tání zvětšuje svůj objem a při tuhnutí ho zmenšuje. Existují ale látky (antimon, bismut,..), které při tání svůj objem zmenšují a při tuhnutí zvětšují.
Anomálie vody
Voda má největší hustotu při 4°C! voda teplá 4°C se drží u dna. Objem vody se při tuhnutí zvětšuje:
Sublimace a desublimace
Fyzikální děj, při kterém se mění skupenství látky z pevného na plynné – sublimace a naopak – desublimace (př: jinovatka). Sublimující látky za normálního tlaku: jód, naftalen, kofein, suchý led.
Skupenské teplo sublimace
Teplo, které přijme pevná látka při přechodu v plyn během sublimace.
Měrné skupenské teplo sublimace
Teplo, které musíme dodat 1 kg látky, aby změnila své skupenství z pevného na plynné.
Vypařování a kondenzace
Fyzikální děj, při kterém se mění skupenství látky z kapalného na plynné – vypařování a naopak – kondenzace/kapalnění. Vypařování z povrchu kapaliny probíhá za každé teploty. Rychlost vypařování se zvyšuje s teplotou kapaliny a s obsahem jejího povrchu.
- Sytá pára
- Pára v rovnovážném vztahu se svou kapalinou, vypařená látka je přesně nahrazena látkou zkondenzovanou.
- Var
- Stav, kdy se kapalina vypařuje v celém svém objemu
Skupenské teplo varu
Teplo, které přijme kapalina při přechodu v plyn během varu.
Měrné skupenské teplo varu
Teplo, které musíme dodat 1 kg látky, aby změnila své skupenství z kapalného na plynné.
Fázový diagram
Existují rovnovážní stavy mezi skupenstvími téže látky a tyto všechny rovnovážné stavy můžeme znázornit ve fázovém diagramu.
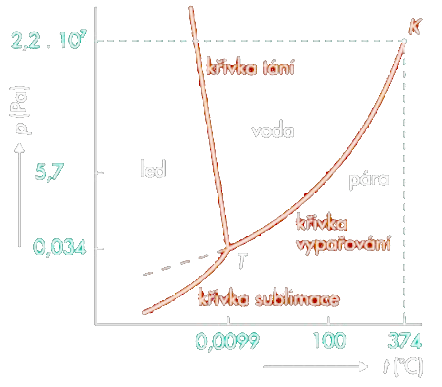
- Bod – trojný bod – znázorňuje rovnovážný stav všech tří skupenství
- Bod – kritický bod – v tomto bodě mizí rozdíl mezi kapalinou a párou
Vodní pára v atmosféře
Vodní pára je vždy v dolních vrstvách zemské atmosféry. Charakteristickou vlastností vzduchu je jeho vlhkost, tj. kolik vodní páry obsahuje.
Absolutní vlhkost vzduchu
Označuje hmotnost vodní páry ve vzduchu. Značka . Jednotka [g.m].
Vodní pára ve vzduchu bývá přehřátá. Pokud se ale stane za určité teploty sytou párou, tak absolutní vlhkost vzduchu dosáhne maximální hodnoty
Relativní vlhkost vzduchu
Udává, jak moc se stav vodní páry ve vzduchu liší od stavu syté vodní páry. Značka je . Udává se v procentech.
